A contaminação dos endoscópios é realmente um problema?
Foram associadas mais infeções nosocomiais e surtos de pseudo-infeções a endoscópios contaminados que a qualquer outro dispositivo médico.1
Os resultados de uma investigação realizada por uma comissão do Senado dos EUA comprova que, entre 2012 e a primavera de 2015, os endoscópios causaram pelo menos 250 infeções perigosas em todo o mundo, incluindo infeções com a enterobactéria resistente a carbapenem.2
A contaminação e a limpeza inadequada dos endoscópios foram reconhecidas como um sério problema para a segurança do paciente por parte da ECRI - uma organização americana não lucrativa focada na melhoria da segurança do paciente. Por conseguinte, a lista anual da ECRI de "10 principais perigos da tecnologia da saúde” tem vindo a incluir continuamente este problema ao longo dos últimos 9 anos.3
Risco de biofilm em endoscópios reutilizáveis
Os procedimentos de limpeza de rotina não removem o biofilme de forma fiável dos canais endoscópicos.21
Por conseguinte, a implementação do controlo de infeções através da vigilância microbiológica do reprocessamento de endoscópios é adequada para detetar a formação precoce de colonização e biofilme no endoscópio e para prevenir a contaminação e infeção em pacientes após procedimentos endoscópicos.22
A FDA exige o controlo de infeções
A 12 de março de 2015, a U.S. Food and Drug Administration anunciou novas ações para aumentar a segurança dos dispositivos médicos reutilizáveis e abordar a possível disseminação de agentes infecciosos.4, 5, 6
Comunicação de segurança sobre broncoscópios pela FDA
Desde então, a FDA emitiu novas orientações sobre o reprocessamento de dispositivos médicos, organizou um seminário de 2 dias sobre a transmissão de infeções associadas a endoscópios, emitiu avisos aos fabricantes de duodenoscópios relativamente à falta de preenchimento de relatórios sobre MDR, além de ter emitido uma comunicação de segurança sobre a infeção associada a broncoscópios flexíveis reprocessados.6
Intervenções da FDA
Março de 2015:
Novas orientações sobre o reprocessamento de dispositivos médicos
Maio de 2015:
Seminário de 2 dias para resolver problemas com endoscópios contaminados
Agosto de 2015:
Necessidade da realização de estudos de vigilância pós-venda aos endoscópios
Agosto de 2015:
Avisos para os fabricantes de duodenoscópios
Setembro de 2015:
Comunicação de segurança sobre broncoscópios
Novembro de 2016:
Dois pacientes morreram devido a broncoscópio contaminado numa instalação americana7
Janeiro de 2017:
O registo de MDR relativo a broncoscópios contaminados bate records com a comunicação de 183 MDR à FDA em 2016
Janeiro de 2018:
O registo de MDR relativo a broncoscópios contaminados bate um novo record com a comunicação de 215 MDR à FDA em 2017
Março de 2018:
A FDA adverte os fabricantes de duodenoscópios sobre a não realização de estudos de vigilância pós-venda para avaliar os riscos de contaminação
Aumento contínuo da não conformidade com uma norma de controlo de infeções destinada a reduzir o risco de infeção
IC.02.02.01 Não conformidade dos hospitais nos EUA
A Comissão Conjunta acredita e certifica quase 21.000 organizações de cuidados de saúde e programas nos Estados Unidos.
A Norma da Comissão Conjunta IC.02.02.01: exige que as organizações reduzam o risco de infeções associadas a equipamento, dispositivos e consumíveis médicos. Desde 2009, tem havido um aumento contínuo da não conformidade com a IC.02.02.01, uma vez que o equipamento está inadequadamente desinfetado a nível elevado (HLD) e esterilizado.
"Relativamente a este assunto, a Comissão Conjunta concluiu que, entre 2013 e 2016, as declarações de perigo de vida imediato (ITL) relacionadas com equipamento inadequadamente esterilizado ou HDL aumentaram significativamente. Em 2016, 74% de todos os perigos de vida imediatos estiveram relacionados com equipamento inadequadamente esterilizado ou HDL." 23
Os broncoscópios infetados constituem um desafio particular
Os broncoscópios flexíveis são difíceis de limpar e desinfetar devido aos seus lúmens longos e estreitos e aos materiais delicados. A dúvida é se é possível garantir a desinfeção a 100% de cada dispositivo. Apesar de terem sido cumpridas as instruções de limpeza, tem-se observado uma contaminação persistente do dispositivo, e é provável que a falta de rigor no cumprimento das instruções de limpeza resulte na contaminação dos dispositivos.6, 8
A limpeza de rotina não é suficiente
É provável que seja pouco reconhecida a verdadeira incidência de contaminação cruzada e de infeção durante a broncoscopia flexível, devido a uma informação deficiente e a uma vigilância inadequada ou inexistente.8, 9
Numa visão geral das infeções associadas à broncoscopia flexível desde 2013, foram identificados 50 estudos. Em 30 dos 50 estudos publicados, descobriu-se o mesmo contaminante no paciente e no broncoscópio. Um total de 569 pacientes contaminados e 115 pacientes infetados (20,21%) podem estar diretamente relacionados com broncoscópios contaminados.8
A limpeza de rotina não remove eficazmente o biofilme dos canais endoscópicos. O biofilme esteve presente em 13 dos 13 endoscópios, apesar de terem sido seguidos os procedimentos de limpeza adequados nos canais de 12 dos 13 instrumentos.10
Do mesmo modo, um outro estudo verificou o crescimento microbiano em 32 de 45 endoscópios (71%).17
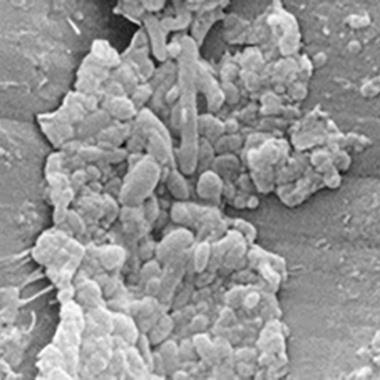
Sujidade e microrganismos nos canais de aspiração
Micrografias eletrónicas de um canal de aspiração que apresentam defeitos na superfície.
A sujidade biológica está associada aos defeitos e também está presa a áreas não danificadas.

Uma ampliação de uma das áreas defeituosas que mostra sujidade e diversos tipos de microrganismos.
Sujidade e biofilme nos canais de ar/água
Micrografias eletrónicas de dois canais de ar/água diferentes com biofilmes.
Uma vista de baixa potência que mostra uma camada confluente de sujidade e biofilme.
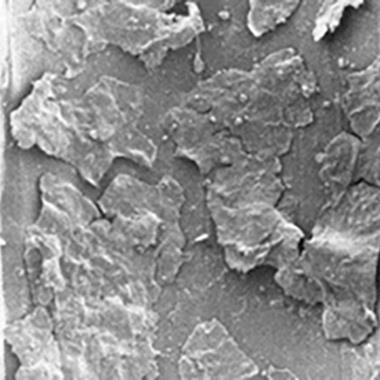
Um biofilme multicamadas composto por células de aspeto saudável rodeadas e sobrepostas por exopolissacarídeos amorfos.

Está a aumentar o risco de estirpes de bactérias resistentes.
Há muitos anos que os intensivistas, enfermeiros de higiene e outros envolvidos no controlo de infeções estão cientes do risco de contaminação e infeção dos pacientes sujeitos a cuidados médicos. A chegada de Organismos resistentes a múltiplos fármacos (MDRO), como o CRE ou os Pseudomonas aeruginosa resistente a múltiplos fármacos, constitui um novo desafio quando se trata dos riscos envolvidos para os pacientes, médicos, hospitais e clínicas.
Foram relatados surtos de organismos resistentes a fármacos causados por broncoscópios reutilizáveis.18,19,20
Veja o vídeo que demonstra como os broncoscópios representam um risco particular de contaminação cruzada do paciente.
Impacto financeiro da contaminação cruzada
A quantificação dos resultados de uma pesquisa de literatura sistemática revelou uma contaminação geral de broncoscópios de 8,7%.* A análise inclui 1664 amostras de 13 estudos realizados em 8 países diferentes.25-37
Como a maioria dos pacientes contaminados por broncoscópios sofre de pneumonia8,13 os custos relativos à pneumonia associada a um ventilador (25.149 USD) são usados como o impacto clínico no cálculo dos custos. Combinando os 8% de risco de contaminação cruzada com os 20,21% de risco de infeção, é possível calcular o custo associado à contaminação cruzada:
0,08 x 0,2021 x 25.149 = 407 USD*
*Dependendo das fontes, risco de contaminação e infeções mais o custo da PAV.
8% de risco de contaminação cruzada25-37 vezes o risco de uma infeção (cálculo baseado em Kovaleva et al.8) vezes o custo de uma pneumonia associada a ventilador 25.149 USD.38
Num recente surto de Pseudomonas, calculou-se que os custos com cuidados de saúde diretamente relacionados com o diagnóstico, o tratamento e o internamento de seis pacientes afetados tenham sido de 243.000 USD ou 40.500 USD por paciente.14

Esterilidade garantida. Pronto quando você estiver.
Os surtos levaram os médicos a questionarem-se sobre a segurança da broncoscopia. Os endoscópios, incluindo os broncoscópios, são os dispositivos médicos mais frequentemente associados a surtos de infeções nosocomiais.15, 16
O risco de infeção cruzada com micróbios multirresistentes na UCI durante os procedimentos de broncoscopia de cabeceira pode ser significativamente reduzido através da utilização de um broncoscópio de uso único estéril.
O sistema aScope 4 Broncho de uso único da Ambu minimiza o risco de contaminação cruzada ao assegurar a esterilidade diretamente a partir da embalagem, evitando, assim, o biofilme residual causado pelo reprocessamento automático inadequado do endoscópio.
Referências
Diretriz CDC 2008. Desinfeção e esterilização em instalações de cuidados de saúde.
Relatório do Senado dos EUA, 13 de janeiro de 2016 Tragédias evitáveis: Super bactérias e como a monitorização ineficaz da segurança de um dispositivo médico constitui um fracasso para os pacientes
Instituto ECRI https://www.ecri.org/Pages/default.aspx
Notas de imprensa da FDA. A FDA publica as orientações finais sobre o reprocessamento de dispositivos médicos reutilizáveis. 12 de março de 2015.
Reprocessamento de dispositivos médicos em instalações de cuidados de saúde: Métodos de validação e rotulagem. Orientações para os colaboradores da indústria e da Food and Drug Administration. FDA. 17 de março de 2015.
Ir para o artigo: Infeções associadas a broncoscópios flexíveis reprocessados: Comunicação de segurança da FDA
Ir para: Base de dados MAUDE da FDA
Kovaleva et al. 2013; Transmissão de infeções por endoscopia gastrointestinal flexível e broncoscopia. Microbiologia clínica Rev. abril de 2013 vol. 26 n.º 2, p. 231-254
MM. Mughal et al.2004; Reprocessamento do broncoscópio: Os desafios, Seminários sobre medicina respiratória e de cuidados críticos. Vol. 25 n.º 4, p. 443-449
Pajkos et al. A acumulação de biofilme no tubo endoscópio contribui para as falhas de limpeza e descontaminação? Journal of Hospital Infection 2004, 58:224-229.
Terjesen et al. 2017; Avaliação precoce da provável rentabilidade económica dos broncoscópios de vídeo flexíveis de uso único
Michelle Alfa Ph.D.; Testes de verificação do reprocessamento de endoscópios, Apresentação, Materiais da reunião não produzidos pela FDA, Reunião da Comissão da FDA, 14 a 15 de maio de 2015
R. Douglas Scott II, O custo médico direto das infeções associadas a cuidados de saúde nos hospitais americanos e os benefícios da prevenção, Departamento de promoção da qualidade nos cuidados de saúde, Centro nacional para a prevenção, deteção e controlo de doenças infecciosas, Centros para controlo e prevenção de doenças, Março de 2009
Kovaleva et al. Utilidade da monitorização bacteriológica do reprocessamento dos endoscópios, Endoscopia gastrointestinal terapêutica, Cap. 9, p. 141-162, 2011
Srinivasan et al. Um surto de infeções de Pseudomonas aeruginosa associadas a broncoscópios flexíveis. The New England Journal of Medicine, 2003; 348;221-7
Publicação CDC da Healthcare Infection Control Practices Advisory Committee (HICPAC) 25 de janeiro de 2017. "Elementos essenciais de um programa de reprocessamento para endoscópios flexíveis – Recomendações da HICPAC”
Cori L. Ofstead et al 2018; Humidade residual e patogénicos transportados pela água no interior de endoscópios flexíveis: Evidências de um estudo realizado em múltiplos locais e relativo à eficácia da secagem de endoscópios
T. Waite et al 2016; Pseudo-surtos de Stenotrophomonas maltophilia numa unidade de cuidados intensivos em Inglaterra.
Janine Zweigner et al 2014; Um surto de Klebsiella pneumoniae resistente a carbapenem após broncoscopia
T Agerton et al 1997; Transmissão de uma estirpe altamente resistente a fármacos (estirpe W1) de Mycobacterium tuberculosis (bacilo de Koch). Surto comunitário e transmissão nosocomial através de um broncoscópio contaminado.
Ofstead et al 2017: Avaliação longitudinal da eficácia do reprocessamento para colonoscópios e gastroscópios: Resultados de inspeções visuais, marcadores bioquímicos e culturas microbianas
Kovaleva e Buss: Utilidade da monitorização bacteriológica do reprocessamento de endoscópios
A Comissão Conjunta: Quick Safety Edição 33 de maio de 2017
Ofstead et al. 2018 “Eficácia do reprocessamento de broncoscópios flexíveis e broncoscópios de ultrassons endobronquiais” CHEST
M. Guy et al. “Surto de infeções Pseudomonas aeruginosa e Stenotrophomonas maltophilia pulmonares relacionadas com válvulas de aspiração de broncoscópios contaminados” Revista europeia de epidemiologia, prevenção e controlo de doenças infecciosas Eurosurveillance, Volume 21, Edição 28, 14 de julho de 2016
C. Ofstead et al 2016 “Kit de ferramentas prático para monitorização da eficácia do reprocessamento de endoscópios: Identificação de bactérias viáveis em gastroscópios, colonoscópios e broncoscópios.”
Cori L. Ofstead et al. 2018 “Humidade residual e patogénicos transmitidos pela água no interior de endoscópios flexíveis: Evidências de um estudo realizado em múltiplos locais e relativo à eficácia da secagem de endoscópios."
P. Batailler et al 2015 “Utilidade do Estudo de bioluminescência do trifosfato de adenosina (ATPmetry) para monitorização do reprocessamento de endoscópios.”
M. Botana-Rial et al 2016 “Um pseudo-surto de Pseudomonas putida e Stenotrophomonas maltophilia numa unidade de broncoscopia.”
C. DiazGranados et al 2009 “Surto de infeção de Pseudomonas aeruginosa associada à contaminação de um broncoscópio flexível”
L. Gavaldà et al 2015 “Monitorização microbiológica de broncoscópios flexíveis após a desinfeção a alto nível e a lavagem dos canais com álcool: Resultados e custos”
T. Guimarães et al 2016 “Pseudo-surto de uma micobactéria de crescimento rápido devido a um Mycobacterium abscessus subsp bolletii numa unidade de endoscopia digestiva e respiratória causada pelo mesmo clone que o de um surto de âmbito nacional”
M. Marino et al 2012 “O reprocessamento após a não utilização é um procedimento de segurança para a broncoscopia?”
D. Rosengarten et al 2010 “Aglomerado de pseudo-infeções com Burkholderia cepacia associadas a um dispositivo de lavagem/desinfeção contaminado numa unidade de broncoscopia”
N. Shimono et al 2008 “Um surto de infeções de Pseudomonas aeruginosa após cirurgias torácicas que ocorrem através da contaminação de broncoscópios e um preprocessador de endoscópios automáticos.”
S. Vincenti et al 2014 “Bactéria gram-negativa não-fermentativa em água de torneira de um hospital e água usada para hemodiálise e lavagem de broncoscópios: Prevalência e distribuição de estirpes resistentes a antibióticos ”
T.D. Waite et al “Pseudo-surtos de Stenotrophomonas maltophilia numa unidade de cuidados intensivos em Inglaterra.”
R. Douglas 2009 “Os custos médicos diretos de infeções associadas a cuidados de saúde em hospitais americanos e os benefícios da prevenção”

